1. ใส่น้ำกลั่น 10 cm3ลงในหลอดทดลองขนาดกลาง ทดสอบการนำไฟฟ้าด้วยเครื่องตรวจการนำไฟฟ้า สังเกตความสว่างของหลอดไฟ
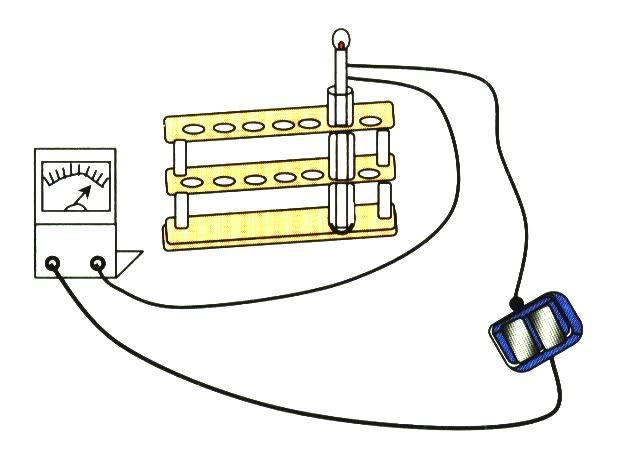
2. ต่อแอมมิเตอร์ชนิดที่นำไฟฟ้าได้เป็นไมโครแอมแปร์เข้ากับเครื่องตรวจการนำไฟฟ้า แล้วจุ่มลวดตัวนำของเครื่องตรวจการนำไฟฟ้าลงในน้ำกลั่น ดังรูป อ่านค่ากระแสไฟฟ้า บันทึกผล
3. อุ่นน้ำกลั่นให้ร้อนประมาณ 60 cแล้วทดสอบการนำไฟฟ้าเช่นเดียวกับข้อ 2
 ผลการทดลอง
ผลการทดลองน้ำบริสุทธิ์นำไฟฟ้าได้น้อยมาก จนไม่สามารถตรวจสอบได้ดัวยเครื่องตรวจการนำไฟฟ้าธรรมดา แต่เมื่อใช้แอมมิเตอร์ช่วยในการทดสอบ เข็มของแอมมิเตอร์เบนเล็กน้อย แสดงว่าน้ำบริสุทธิ์แตกตัวให้ไฮโดรเนีบมไอออนและไฮดรอกไซด์ไอออนน้อยมาก การแตกตัวของน้ำบริสุทธิ์เป็นดังสมการ
เนื่องจากน้ำแตกตัวได้น้อยมากจนถือว่าความเข้มข้นของน้ำไม่เปลี่ยนแปลง เมื่อจัดความสัมพันธ์อยู่ในรูปใหม่ จึงได้ค่าคงที่ใหม่ซึ่งเรียกว่า ค่าคงที่การแตกตัวของน้ำ ใช้สัญลักษณ์ Kw
ดังนั้นKw= [H3O+][OH-]
จากผลการทดลอง พบว่าน้ำที่อุณหภูมิสูงนำไฟฟ้าได้ดีกว่าที่อุณหภูมิต่ำ แสดงว่าน้ำที่อุณหภูมิสูงแตกตัวเป็นไอออนได้มากกว่าที่อุณหภูมิต่ำKwจึงสูงกว่า ตัวอย่างเช่น
ค่า ที่อุณหภูมิ 25cมีค่าเท่ากับ 1.0 x 10-14mol/dm3
ค่า ที่อุณหภูมิ 60 cมีค่าเท่ากับ 9.5 x 10-14mol/dm3
ค่า ที่อุณหภูมิ 60 cมีค่าเท่ากับ 9.5 x 10-14mol/dm3
ดังนั้น การบอกค่าKwจึงต้องระบุอุณหภูมิด้วยเช่นเดียวกับค่าคงที่อื่นๆ โดยปกติเราไม่กล่าวถึงหน่วยของ Kwเช่นเดียวกับค่าคงที่สมดุลอื่นๆ ยกเว้นในกรณีที่จะนำมาใช้คำนวณความเข้มข้นของไอออนที่ระบุหน่วยของ Kw
จากสมการการแตกตัวของน้ำ จะได้ไฮโดรเนียมไอออนและไฮดรอกไซด์ไอออนเกิดขึ้นในจำนวนโมลที่เท่ากัน ดัวนั้น
=[OH- ]นั่นคือKw=[H3O+]2หรือ [OH-]2
=[OH- ]นั่นคือKw=[H3O+]2หรือ [OH-]2
[H3O+]
หรือ[H3O+] =[OH-] =Kw
หรือ[H3O+] =[OH-] =Kw
=[OH-] =1.0 x 10-14 mol2/dm6 ณ อุณหภูมิ 25 c
[H3O+]
=1.0 x 10-7 mol/dm3
แสดงว่าน้ำบริสุทธิ์ที่อุณหภูมิ 25 cมีความเข้มข้นของไฮดรอกไซด์ไอออน คือ1.0 x 10-7
แสดงว่าน้ำบริสุทธิ์ที่อุณหภูมิ 25 cมีความเข้มข้นของไฮดรอกไซด์ไอออน คือ1.0 x 10-7

การทดลองที่ 2 ปฎิกิริยาระหว่างกรดหรือเบสกับสารบางชนิด
ตอนที่ 1 ปฎิกิริยาระหว่าง HCL กับ CaCO3
1. นำหินอ่อนประมาณ 5 กรัม ล้างน้ำให้สะอาด แล้วใส่ในหลอดทดลองขนาดกลาง
2. เติมสารละลายกรดไฮโดรคลอริกเข้มข้น 1.0 mol/dm35cm3ปิดด้วยจุกยางที่มี หลอดนำแก๊สเสียบอยู่ทันที ผ่านแก๊สที่ได้ลงในน้ำปูนใส สังเกตการเปลี่ยนแปลง
3. เมื่อสิ้นสุดปฎิกิริยา รินสารละลายจากหลอดทดลองในข้อ 2 ใส่ในถ้วยกระเบื้อง ระเหยให้แห้งบันทึกผล
ตอนที่ 2 ปฎิกิริยาระหว่าง NaOH กับ FeCl3
1. ใส่สารละลาย NaOH เข้มข้น 1.0 mol/ dm3 3 cm3ลงในหลอดทดลองขนาดกลาง
2. เติมสารละลาย FeCl2เข้มข้น 1.0mol/dm33 cm3ลงในสารละลายข้อที่ 1 เขย่า สังเกตการเปลี่ยนแปลง บันทึกผล
3. กรองสารในข้อ 2 แล้วนำของเหลวที่กรองได้ไประเหยในถ้วยกระเบื้อง บันทึกผล
ผลการทดลอง
การทดลองตอนที่ 1 เมื่อผสมสารละลายกรดไฮโดรคลอริกกับแคลเซียมคาร์บอเนตจะได้ฟองแก๊สเกิดขึ้น ซึ่งทดสอบได้ว่าเป็นแก๊สคาร์บอนไดออกไซด์ เมื่อนำส่วนที่เป็นของเหลวไประเหยแห้ง จะได้ของแข็งสีขาวซึ่งคือ แคลเซียมคลอไรด์ ปฎิกิริยาที่เกิดขึ้นสามารถเขียนสมการได้ดังนี้
การทดลองตอนที่ 1 เมื่อผสมสารละลายกรดไฮโดรคลอริกกับแคลเซียมคาร์บอเนตจะได้ฟองแก๊สเกิดขึ้น ซึ่งทดสอบได้ว่าเป็นแก๊สคาร์บอนไดออกไซด์ เมื่อนำส่วนที่เป็นของเหลวไประเหยแห้ง จะได้ของแข็งสีขาวซึ่งคือ แคลเซียมคลอไรด์ ปฎิกิริยาที่เกิดขึ้นสามารถเขียนสมการได้ดังนี้
การทดลองตอนที่ 2 เมื่อผสมสารละลายโซเดียมไฮดรอไซด์กับสารละลายไอร์ออน (III) คลอไรด์ จะได้ตะกอนสีน้ำตาลคล้ายวุ้นซึ่งคือไอร์ออน (III) ไฮดรอกไซด์ เมื่อนำส่วนที่เป็นของเหลวในหลอดไประเหยแห้ง จะได้ของแข็งสีขาว ปฎิกิริยาที่เกิดขึ้นเขียนสมการได้ดังนี้
จึงสรุปได้ว่าการทดลองทั้งสองตอนนี้ ได้ผลิตภัณฑ์เป็นสารประกอบของเกลือที่ละลายได้ในน้ำ
นอกจากนี้ยังมีสารอื่นที่สามารถทำปฎิกิริยากับกรดหรือเบสแล้วได้เกลือเกิดขึ้น เช่น โลหะแมกนีเซียมกับกรดไฮโดรคลอริก จะได้แมกนีเซียมคลอไรด์กับแก๊สไฮโดรเจน โลหะทองแดงกับกรดไนตริกเข้มข้นได้คอปเปอร์ (II) ไนเตรตกับแก๊สไนโตรเจนไดออกไซด์ ซึ่งได้ศึกษามาแล้ว นอกจากนี้โลหะบางชนิดก็สามารถทำปฎิกิริยาได้ทั้งกรดและเบส เช่น สังกะสีและอะลูมิเนียม
สามารถทำปฎิกิริยากับกรดไฮโดรคลอริกและสารละลายโซเดียมไฮดรอไซด์ได้แก๊สไฮโดรเจน
กรดและเบสนอกจากจะทำปฎิกิริยาโดยตรงแล้ว ทั้งกรดและเบสยังสามารถทำปฏิกิริยากับสารอื่นได้ด้วย และได้สารประกอบประเภทเกลือตามชนิดของกรดและเบสหรือชนิดของสารตั้งต้นที่เข้าทำปฏิกิริยากัน เมื่อพิจารณาสูตรสารประกอบของเกลือชนิดต่างๆ พบว่าประกอบด้วยไอออนบวกและไอออนลบ เกลือจึงเป็นสารประกอบไอออนิกที่ประกอบด้วยไอออนบวกที่ไม่ใช่H+และไอออนลบที่ไม่ใช่ OH-หรือO2- เกลือทุกชนิดเป็ยสารอิเล็กโทรไลต์แก่ แต่สารประกอบของเกลือบางชนิดละลายได้ในน้ำ
กรดและเบสนอกจากจะทำปฎิกิริยาโดยตรงแล้ว ทั้งกรดและเบสยังสามารถทำปฏิกิริยากับสารอื่นได้ด้วย และได้สารประกอบประเภทเกลือตามชนิดของกรดและเบสหรือชนิดของสารตั้งต้นที่เข้าทำปฏิกิริยากัน เมื่อพิจารณาสูตรสารประกอบของเกลือชนิดต่างๆ พบว่าประกอบด้วยไอออนบวกและไอออนลบ เกลือจึงเป็นสารประกอบไอออนิกที่ประกอบด้วยไอออนบวกที่ไม่ใช่H+และไอออนลบที่ไม่ใช่ OH-หรือO2- เกลือทุกชนิดเป็ยสารอิเล็กโทรไลต์แก่ แต่สารประกอบของเกลือบางชนิดละลายได้ในน้ำ
 การทดลองที่ 3 การไทเทรตหาจุดยุติของปฎิกิริยาระหว่างกรดแก่กับเบสแก่
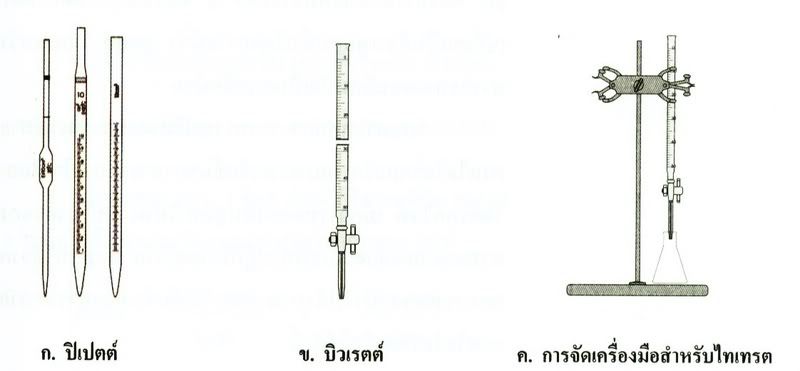
การทดลองที่ 3 การไทเทรตหาจุดยุติของปฎิกิริยาระหว่างกรดแก่กับเบสแก่1. ปิเปตต์สารละลาย HCl 10.0 cm3ใส่ขวดรูปกรวยขนาด 100cm3วัด pH ของสารละลาย HCl โดยใช้กระดาษ pH บันทึกแล้วหยดฟีนอล์ฟทาลีนลงไป 2-3 หยด
2. บรรจุสารละลายโซเดียมไฮดรอกไซด์ เข้มข้น 0.1 mol/dm3บิวเรตต์ ไข สารละลายให้เต็มปลายล่างของบิวเรตต์และปรับระดับของสารละลายให้ตรงกับขัดใดขีดหนึ่ง บันทึกปริมาตรไว้
3. หยดสารละลาย NaOH จากบิวเรตต์ลงในสารละลาย HCl ที่อยู่ในขวดรูปกรวยทีละหยด พร้อมกับเขย่าขวดให้สารละลายผสมกัน ทำเช่นนี้จนกระทั่งสารละลายเริ่มเปลี่ยนเป็นสีชมพูอ่อนอย่างถาวร บันทึกปริมาตรของสารละลาย NaOH และวัดpH ของสารละลายผสมด้วยกระดาษ pH
4. ทดลองซ้ำข้อ 1-3 อีก 2 ครั้ง บันทึกผล
5. หาปริมาตรเฉลี่ยของสารละลาย NaOH ที่ใช้ทำปฏิกิริยาพอดีกับสารละลาย HCl
ผลการทดลอง
ในการทดลองนี้สารละลาย HCl มีสมบัติเป็นกรด ( เมื่อหยดฟีนอล์ฟทาลีนจึงไม่ปรากฏสี )เมื่อหยด NaOH ลงไป OH-จากเบสจะทำปฏิกิริยากับ H3Oจากกรด ทำให้ pH ของสารละลายเพิ่มขึ้นเรื่อยๆ จนในที่สุดอินดิเคเตอร์เปลี่ยนเป็นสีชมพูอ่อนซึ่งเรียกภาวะนี้ว่า จุดยุติ และพบว่าสารละลายผสมมีสมบัติเป็นเบสเล็กน้อย
ก่อนการทดลอง เราทราบปริมาตรของสารละลายกรดไฮโดรคลอริก และความเข้มข้นของสารละลายโซเดียมไฮดรอกไซด์ เมื่อการทดลองสิ้นสุดทำให้ทราบปริมาตรของสารละลายกรดและเบสที่ทำปฏิกิริยาพอดีกัน ข้อมูลที่ได้จากผลการทดลองนำไปคำนวณหาความเข้มข้นของสารละลายกรดไฮโดรคลอริกได้ดังนี้
สมมติให้สารละลาย NaOH 0.1 mol/dm3 จำนวน V cm3ทำปฏิกิริยาพอดีกับสารละลาย HCl a mol/dm3 จำนวน 10cm3
จำนวนโมลของ NaOH ในสารละลาย 0.1 mol/dm3 ปริมาตร Vcm3เป็นดังนี้
= NaOH 0.1 mol สารละลาย 1 dm3 สารละลาย V cm3
สารละลาย 1 dm3สารละลาย 1000 cm3
= NaOH 0.1 V mol
1000
จำนวนโมลของ NaOH ในสารละลาย 0.1 mol/dm3 ปริมาตร Vcm3เป็นดังนี้
= NaOH 0.1 mol สารละลาย 1 dm3 สารละลาย V cm3
สารละลาย 1 dm3สารละลาย 1000 cm3
= NaOH 0.1 V mol
1000
สมมติให้สารละลาย HCl มีความเข้มข้น a mol/ dm3 จำนวนโมลของ HCl ในสารละลายเข้มข้น a mol/dm3 ปริมาตร 10cm3เป็นดังนี้
= HCl a mol สารละลาย 1dm3 สารละลาย 10dm3
สารละลาย 1dm3สารละลาย 1000cm3
= HCl 10a mol
1000
= HCl a mol สารละลาย 1dm3 สารละลาย 10dm3
สารละลาย 1dm3สารละลาย 1000cm3
= HCl 10a mol
1000
ปฏิกิริยาที่เกิดขึ้นระหว่าง HCl กับ NaOH เป็นดังนี้
จากสมการ HCl 1 โมล ทำปฏิกิริยาพอดีกับ NaOH 1 โมล นั่นคือ จำนวนโมลของ NaOH เท่ากับ HCl
ดังนั้น 0.1 V mol = 10 a mol
1000 1000
a = 0.1 V
10
ดังนั้น 0.1 V mol = 10 a mol
1000 1000
a = 0.1 V
10
สารละลายกรด HCl มีความเข้มข้น 0.01 V mol/dm3
V เป็นค่าที่ได้จากการทดลอง เมื่อแทนค่า V ทำให้สามารถคำนวณหาความเข้มข้นของสารละลายกรดไฮโดรคลอริกได้
การทดลองที่ 4 เป็นวิธีหาปริมาตรของสารในสารละลายตัวอย่าง โดยให้ทำปฏิกิริยากับสารละลายที่ทราบความเข้มข้น และวัดปริมาณของสารละลายทั้งสองที่ทำปฏิกิริยาพอดีกัน กระบวนการหาปริมาณของสารโดยวิธีนี้เรียกว่าการ ไทเทรต และการทดลองนี้ใช้การเปลี่ยนสีของอินดิเคเตอร์ในการบอกจุดยุติของการไทเทรต
ในการไทเทรตจำเป็นต้องทราบความเข้มข้นของสารละลายหนึ่ง แล้วคำนวณหาความเข้มข้นของสารละลายอีกชนิดหนึ่ง สารละลายที่ทราบความเข้มข้นแน่นอนเรียกว่า สารละลายมาตรฐาน นอกจากนี้ต้องทราบภาวะที่กรดกับเบสทำปฏิกิริยาพอดีกัน ซึ่งพิจารณาจากการเปลี่ยนสีของอินดิเคเตอร์ที่เติมลงไป ดังนั้นการเลือกอินดิเคเตอร์ที่เหมาะสมจะช่วยในการไทเทรตได้ผลถูกต้องมากที่สุด
การไทเทรตระหว่างสารละลาย HCl กับสารละลาย NaOH จะได้ NaCl และ เป็นผลิตภัณฑ์ ภาวะที่กรดกับเบสทำปฏิกิริยาพอดีกันเรียกว่า จุดสมมูล และได้ทราบมาแล้วว่าสารละลาย NaCl มีสมบัติเป็นกลาง เมื่อสิ้นสุดการไทเทรต สารละลายผสมควรมี pH เท่ากับ 7
แต่จากการทดลองพบว่าภาวะที่อินดิเคเตอร์เปลี่ยนสีซึ่งเป็นจุดยุติ วัด pH ของสารละลายได้ประมาณ 7-8

การทดลองที่ 4 การไทเทรตหาจุดสมมูลของปฏิกิริยาระหว่างกรดกับเบสแก่
1. ปิเปตตสารละลายไฮโดรคลอริกเข้มข้น 0.1 mol/dm3 จำนวน 25cm3ใส่ในขวดรูปกรวยขนาด 100cm3 2. หยดยูนิเวอร์ซัลอินดิเคเตอร์ 5 หยด เขย่าแล้วนำไปเปรียบเทียบสีของยูนิเวอร์ซัลอินดิเคเตอร์ในสารละลายที่มี pH ต่างๆ บันทึกค่า pH ของสารละลาย
3. ไขสารละลายโซเดียมไฮดรอกไซด์เข้มข้น 0.1 mol/dm3 จากบิวเรตต์ลงในสารละลายข้อ 2 ครั้งละ 5cm34 ครั้ง บันทึกค่า pH ของสารละลายผสมทุกครั้งที่เติมสารละลายโซเดียมไฮดรอกไซด์ลงไป
4. เติมสารละลายโซเดียมไฮดรอกไซด์ต่อไปอีก ครั้งละ 1cm3บันทึกค่า pH ทุกครั้งที่เติม และไทเทรตต่อไปจนกระทั่งสารละลายเปลี่ยนเป็นสีม่วงน้ำเงิน วัด pH ของสารละลาย
5. หลังจากจุดยุติแล้วเติมสารละลายโซเดียมไฮดรอกไซด์ครั้งละ 1cm3ต่อไปอีก 3 ครั้ง บันทึกค่า pH
6. เขียนกราฟแสดงความสัมพันธ์ระหว่างค่า pH ของสารละลายกับปริมาตรของโซเดียมไฮดรอกไซด์ที่เติมลงไป
1. ปิเปตตสารละลายไฮโดรคลอริกเข้มข้น 0.1 mol/dm3 จำนวน 25cm3ใส่ในขวดรูปกรวยขนาด 100cm3 2. หยดยูนิเวอร์ซัลอินดิเคเตอร์ 5 หยด เขย่าแล้วนำไปเปรียบเทียบสีของยูนิเวอร์ซัลอินดิเคเตอร์ในสารละลายที่มี pH ต่างๆ บันทึกค่า pH ของสารละลาย
3. ไขสารละลายโซเดียมไฮดรอกไซด์เข้มข้น 0.1 mol/dm3 จากบิวเรตต์ลงในสารละลายข้อ 2 ครั้งละ 5cm34 ครั้ง บันทึกค่า pH ของสารละลายผสมทุกครั้งที่เติมสารละลายโซเดียมไฮดรอกไซด์ลงไป
4. เติมสารละลายโซเดียมไฮดรอกไซด์ต่อไปอีก ครั้งละ 1cm3บันทึกค่า pH ทุกครั้งที่เติม และไทเทรตต่อไปจนกระทั่งสารละลายเปลี่ยนเป็นสีม่วงน้ำเงิน วัด pH ของสารละลาย
5. หลังจากจุดยุติแล้วเติมสารละลายโซเดียมไฮดรอกไซด์ครั้งละ 1cm3ต่อไปอีก 3 ครั้ง บันทึกค่า pH
6. เขียนกราฟแสดงความสัมพันธ์ระหว่างค่า pH ของสารละลายกับปริมาตรของโซเดียมไฮดรอกไซด์ที่เติมลงไป
ผลการทดลอง
เมื่อนำข้อมูลที่ได้จากการไทเทรตระหว่างกรด HCl กับ NaOH มาเขียนกราฟแสดงความสัมพันธ์ระหว่าง pH ของสารละลายผสม กับปริมาตรของสารละลายโซเดียมไฮดรอกไซด์ที่เติมลงไปได้กราฟดังนี้
เมื่อนำข้อมูลที่ได้จากการไทเทรตระหว่างกรด HCl กับ NaOH มาเขียนกราฟแสดงความสัมพันธ์ระหว่าง pH ของสารละลายผสม กับปริมาตรของสารละลายโซเดียมไฮดรอกไซด์ที่เติมลงไปได้กราฟดังนี้
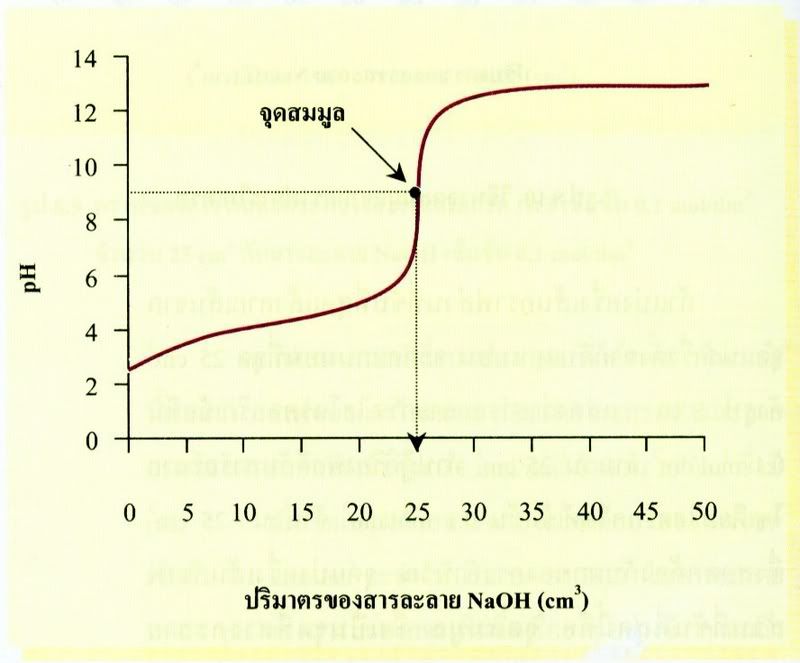
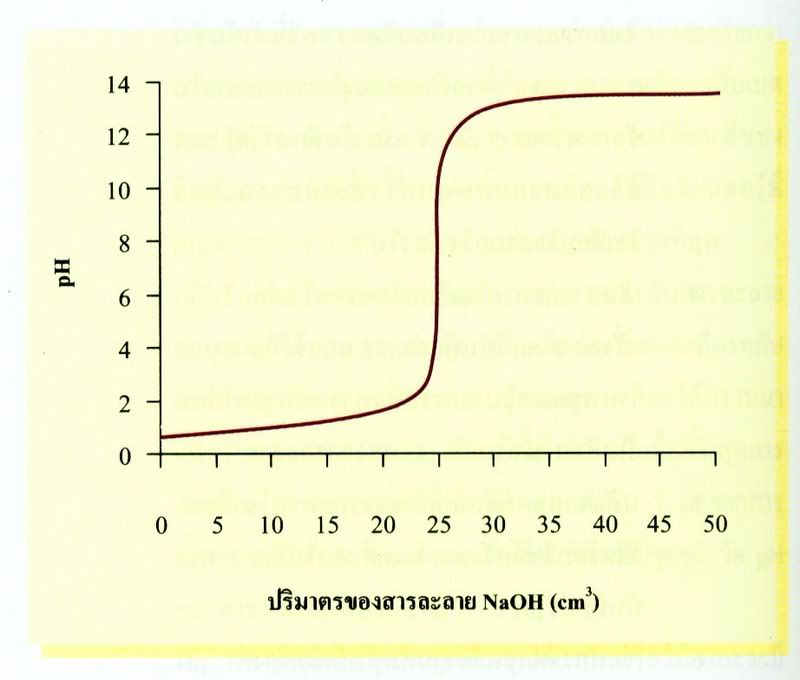 กราฟแสดงการเปลี่ยนแปลง pH ที่ได้จากการไทเทรตนี้เรียกว่า กราฟของการไทเทรต ก่อนการไทเทรตสารละลายกรดไฮโดรคลอริกเข้มข้น 0.1 mol/dm3จำนวน 25cm3ซึ่งมี
กราฟแสดงการเปลี่ยนแปลง pH ที่ได้จากการไทเทรตนี้เรียกว่า กราฟของการไทเทรต ก่อนการไทเทรตสารละลายกรดไฮโดรคลอริกเข้มข้น 0.1 mol/dm3จำนวน 25cm3ซึ่งมีpH = 1 เมื่อไทเทรตด้วยสารละลายโซเดียมไฮดรอกไซด์เข้มข้น 0.1 mol/dm3 จะทำให้ปริมาตรของ H3O+ในสารละลายลดลง pH ของสารละลายจะเพิ่มขึ้นเรื่อยๆ อย่างช้าๆ จนถึงจุดยุติซึ่งเป็นภาวะที่อินดิเคเตอร์เปลี่ยนสี pH ของสารละลายจะเพิ่มขึ้นอย่างรวดเร็ว กราฟช่วงนี้จะมีความชันมากที่สุด และมีช่วง pH 3-11 ณ ภาวะนี้เมื่อเติมสารละลายโวเดียมไฮดรอกไซด์ลงไปเพียงหนึ่งหยดหรือเศษส่วนของหยดเท่านั้น ก็จะทำให้อินดิเคเตอร์เปลี่ยนเป็นสีม่วงน้ำเงิน
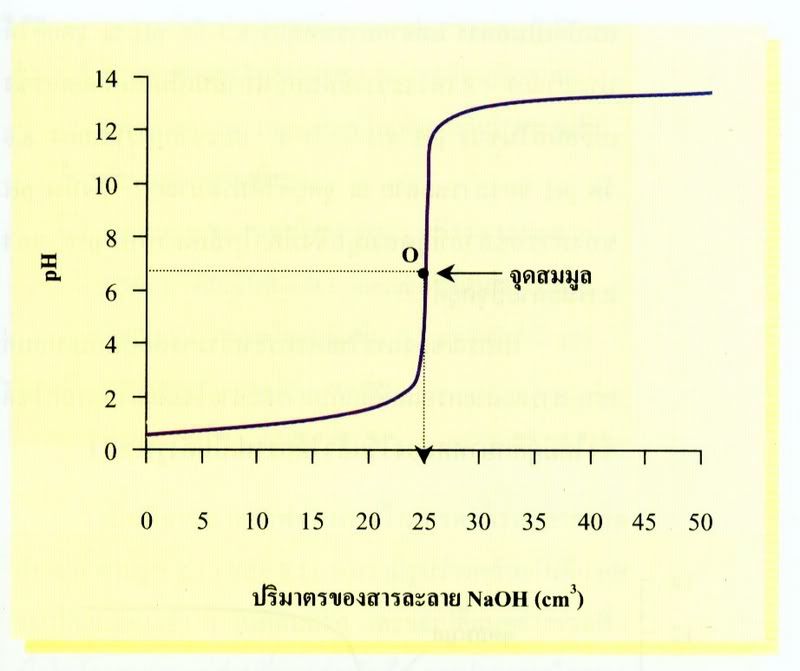 ถ้าแบ่งครึ่งเส้นกราฟส่วนที่ชันที่สุดแล้วลากเส้นจากจุดแบ่งครึ่งตั้งฉากกับแกนนอน จะตัดแกนนอนที่ 25cm3ดังรูป แสดงว่าสารละลายกรดไฮโดรคลอริกเข้มข้น 0.1 mol/dm3จำนวน 25cm3ทำปฏิกิริยาพอดีกับสารละลายโซเดียมไฮดรอกไซด์เข้มข้น 0.1 mol/dm3จำนวน 25cm3ซึ่งสอดคล้องกับผลการคำนวณ จุดแบ่งครึ่งเส้นกราฟ ส่วนที่ชันที่สุดนี้คือ
ถ้าแบ่งครึ่งเส้นกราฟส่วนที่ชันที่สุดแล้วลากเส้นจากจุดแบ่งครึ่งตั้งฉากกับแกนนอน จะตัดแกนนอนที่ 25cm3ดังรูป แสดงว่าสารละลายกรดไฮโดรคลอริกเข้มข้น 0.1 mol/dm3จำนวน 25cm3ทำปฏิกิริยาพอดีกับสารละลายโซเดียมไฮดรอกไซด์เข้มข้น 0.1 mol/dm3จำนวน 25cm3ซึ่งสอดคล้องกับผลการคำนวณ จุดแบ่งครึ่งเส้นกราฟ ส่วนที่ชันที่สุดนี้คือจุดสมมูล ซึ่งเป็นจุดที่สารละลายโซเดียมไฮดรอกไซด์ทำปฏิกิริยาพอดีกับกรดไฮโดรคลอริก
จากจุดสมมูล ถ้าลากเส้นขนานไปกับแกนนอนไปตัดแกนตั้งจะได้ pH เท่ากับ 7 แสดงว่า pH ที่จุดสมมูลของการไทเทรตระหว่างกรดไฮโดรคลอริกกับสารละลายโซเดียมไฮดรอกไซด์มรค่าเท่ากับ 7 สารละลายผสมจึงควรมีสมบัติเป็นกลาง แต่จากการทดลองที่ 3 วัด pH จุดยุติได้ประมาณ 7-8 เพราะว่าใช้ฟีนอล์ทาลีนเป็นอินดิเคเตอร์ซึ่งเปลี่ยนสีในช่วง pH 8.3- 10.0 และจากการทดลองที่ 4 วัด pH ของสารละลาย ณ จุดยุติได้ประมาณ 7 ดังนั้น pH ของสารละลายที่จุดสมมูลจึงมีค่าใกล้เคียงกับ pH ของสารละลายที่จุดยุติ
ในกรณีของการไทเทรตระหว่างกรดอ่อนกับเบสแก่ เช่น สารละลายกรดแอซีติกกับสารละลายโซเดียมไฮดรอกไซด์ เป็นดังกราฟ
 เมื่อพิจารณากราฟของการไทเทรตสารละลายกรดกับเบส ดังรูป พบว่ามีรูปร่างคล้ายกันคือ pH จะเปลี่ยนอย่างช้าๆ ในตอนแรก และจะเปลี่ยนอย่างรวดเร็วเมื่อใกล้จุดสมมูล แต่ส่วนที่แตกต่างกันคือ กราฟการไทเทรตกรดแอซิติกด้วยโซเดียมไฮดรอกไซด์มี pH ที่จุดเริ่มต้นสูงกว่า เนื่องจากกรดแอซีติกเป็นกรดอ่อน และช่วงที่กราฟมีความชันมากที่สุดสั้นกว่าคือช่วง pH 6-11 เมื่อหา pH ที่จุดสมมูลจะได้สูงกว่า 7 คือประมาณ 8.7 ทั้งนี้อธิบายได้ว่า ปฏิกิริยาระหว่างกรดแอซิติกกับโซเดียมไฮดรอกไซด์ จะได้เกลือโซเดียมแอซีเตตเกิดขึ้น
เมื่อพิจารณากราฟของการไทเทรตสารละลายกรดกับเบส ดังรูป พบว่ามีรูปร่างคล้ายกันคือ pH จะเปลี่ยนอย่างช้าๆ ในตอนแรก และจะเปลี่ยนอย่างรวดเร็วเมื่อใกล้จุดสมมูล แต่ส่วนที่แตกต่างกันคือ กราฟการไทเทรตกรดแอซิติกด้วยโซเดียมไฮดรอกไซด์มี pH ที่จุดเริ่มต้นสูงกว่า เนื่องจากกรดแอซีติกเป็นกรดอ่อน และช่วงที่กราฟมีความชันมากที่สุดสั้นกว่าคือช่วง pH 6-11 เมื่อหา pH ที่จุดสมมูลจะได้สูงกว่า 7 คือประมาณ 8.7 ทั้งนี้อธิบายได้ว่า ปฏิกิริยาระหว่างกรดแอซิติกกับโซเดียมไฮดรอกไซด์ จะได้เกลือโซเดียมแอซีเตตเกิดขึ้นCH3COOH (aq) + NaOH(aq)  CH3COOHNa(aq) +H2O (l)
CH3COOHNa(aq) +H2O (l)
CH3COOHNa เมื่อละลายน้ำจะแตกตัวเป็นไอออนได้หมด และCH3COO-ก็จะเกิดปฏิกิริยาไฮโดรไลซิสกับน้ำต่อไปได้ OH-ดังสมการ
CH3COOHNa(aq)  Na+(aq) +CH3COO-(aq)
Na+(aq) +CH3COO-(aq)
CH3COO-(aq) +H2O(l)  CH3COOH(aq) + OH-(aq)
CH3COOH(aq) + OH-(aq)
ดังนั้นการไทเทรตกรดแอซีติกด้วยโซเดียมไฮดรอไซด์ จึงได้สารละลายผสมมีสมบัติเป็นเบส pH ของสารละลายที่จุดสมมูลจึงมีค่ามากกว่า 7
การไทเทรตกรดอ่อนด้วยเบสอ่อน เช่น สารละลายกรดแอซีติกกับแอมโมเนีย จะได้
กราฟของการไทเทรตเป็นดังนี้
กราฟของการไทเทรตเป็นดังนี้
 จากกราฟ จะพบว่าช่วงของการเปลี่ยนแปลง pH ตรงจุดสมมูลสั้นมาก การหาจุดสมมูลจากการไทเทรตระหว่างกรดกับเบสคู่นี้ จึงค่อนข้างยากและไม่เที่ยงตรง ดังนั้นในทางปฏิบัติจึงไม่นิยมการไทเทรตระหว่างกรดอ่อนกับเบสอ่อน
จากกราฟ จะพบว่าช่วงของการเปลี่ยนแปลง pH ตรงจุดสมมูลสั้นมาก การหาจุดสมมูลจากการไทเทรตระหว่างกรดกับเบสคู่นี้ จึงค่อนข้างยากและไม่เที่ยงตรง ดังนั้นในทางปฏิบัติจึงไม่นิยมการไทเทรตระหว่างกรดอ่อนกับเบสอ่อนในการไทเทรตระหว่างกรดกับเบส สิ่งที่สำคัญที่ต้องการทราบก็คือ จุดที่กรดกับเบสทำปฏิกิริยาพอดีกันหรือจุดสมมูล ซึ่งจะหาได้โดยใช้อินดิเคเตอร์ช่วยบอกจุดยุติของการไทเทรต ดังนั้นจึงต้องเลือกใช้อินดิเคเตอร์ให้เหมาะสม เพื่อให้ pH ที่จุดยุติใกล้เคียงกับ pH ของจุดสมมูลมากที่สุด
 การทดลองที่ 5 การเลือกอินดิเคเตอร์ในการไทเทรตกรด-เบส
การทดลองที่ 5 การเลือกอินดิเคเตอร์ในการไทเทรตกรด-เบส1. ปิเปตต์สารละลายCH3COOH0.1 mol/dm3 จำนวน 10cm3ลงในขวดรูปกรวยขนาด 100cm3หยดฟีนอล์ฟทาลีนลงไป 3 หยด
2. บรรจุสารละลาย NaOH 0.1 mol/dm3 ในบิวเรตต์ บันทึกปริมาตรก่อนการไทเทรต
3. หยดสารละลาย NaOH จากบิวเรตต์ลงในสารละลายCH3COOHที่เตรียมไว้ทีละหยด เขย่าขวดทุกครั้งทีหยดลงไป ทำเช่นนี้ต่อไปจนอินดิเคเตอร์เปลี่ยนสี บันทึกปริมาตรของสารละลายในบิวเรตต์
4. ทำการทดลองเช่นเดียวกับข้อ 1-3 แต่ใช้เมทิลออเรนจ์แทนฟีนอล์ฟทาลีน
ผลการทดลอง
จากความรู้ที่ได้ศึกษามาแล้วควรบอกได้ว่า ณ จุดสมมูล ถ้าใช้สารละลายกรดแอซีติกเข้มข้น 0.1 mol/dm3 จำนวน 10cm3จะทำปฏิกิริยาพอดีกับสารละลายโซเดียมไฮดรอกไซด์เข้มข้น 0.1 mol/dm3 จำนวน 10cm3ได้สารละลายที่มีสมบัติเป็นเบส และ pH ที่จุดสมมูลมีค่าประมาณ 8.7
ในการไทเทรตกรดกับเบสคู่นี้ใช้ฟีนอล์ฟทาลีนซึ่งเปลี่ยนสีในช่วง pH 8.3 10.0 และเมทิลออเรนจ์ซึ่งเปลี่ยนสีในช่วง pH 3.2 4.4 เป็นอินดิเคเตอร์ ใช้สารละลายโซเดียมไฮดรอกไซด์มากกว่าเมื่อใช้เมทิลออเรนจ์เป็นอินดิเคเตอร์ แสดงว่าอินดิเคเตอร์ทั้งสองชนิดนี้บอกจุดยุติได้ไม่ตรงกัน ฟีนอล์ฟทาลีนจะบอกจุกยุติได้ใกล้เคียงจุดสมมูลมากกว่า และสามารถเปลี่ยนสีในช่วง pH ที่ตรงกัน pH ของสารละลายเกลือโซเดียมแอซีเตตที่ได้จากปฏิกิริยา ดังนั้นจึงควรใช้ฟีนอล์ฟทาลีนเป็นอินดิเคเตอร์สำหรับการไทเทรตกรด-เบสคู่นี้ กราฟแสดงการไทเทรตระหว่างสารละลาย CH3COOHกับ NaOH
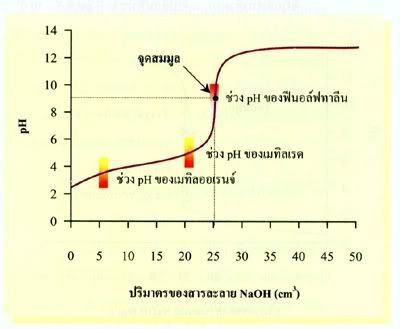 การเลือกใช้อินดิเคเตอร์ที่เหมาะสมสำหรับการไทเทรตกรด-เบส ต้องเลือกใช้อินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนสีใกล้เคียงกับ pH ของสารละลายผลิตภัณฑ์ หรือพิจารณาจากช่วงของการเปลี่ยน pH นั้น ดังตัวอย่างการไทเทรตกรดแก่ดัวยเบสแก่ เช่น HCl กับ NaOH ดังรูป
การเลือกใช้อินดิเคเตอร์ที่เหมาะสมสำหรับการไทเทรตกรด-เบส ต้องเลือกใช้อินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนสีใกล้เคียงกับ pH ของสารละลายผลิตภัณฑ์ หรือพิจารณาจากช่วงของการเปลี่ยน pH นั้น ดังตัวอย่างการไทเทรตกรดแก่ดัวยเบสแก่ เช่น HCl กับ NaOH ดังรูปซึ่งพบว่าช่วงที่ชันที่สุด มีค่า pH 3-11 เราจึงควรเลือกอินดิเคเตอร์ที่เปลี่ยนสีในช่วง pH 3-11 ได้หลายชนิด ได้แก่
เมทิลออเรนจ์ เปลี่ยนสีที่ช่วง pH 3.2 4.4
เมทิลเรด เปลี่ยนสีที่ช่วง pH 4.2 6.3
โบรโมไทมอลบลู เปลี่ยนสีที่ช่วง pH 6.0 7.6
ฟีนอล์ฟทาลีน เปลี่ยนสีที่ช่วง pH 8.3 10.0
เมทิลเรด เปลี่ยนสีที่ช่วง pH 4.2 6.3
โบรโมไทมอลบลู เปลี่ยนสีที่ช่วง pH 6.0 7.6
ฟีนอล์ฟทาลีน เปลี่ยนสีที่ช่วง pH 8.3 10.0
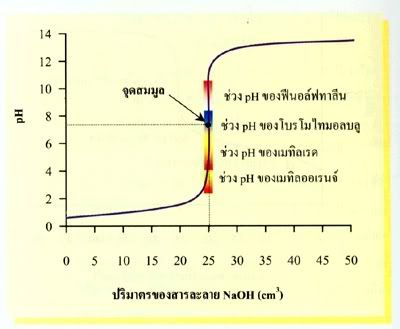 การไทเทรตกรดกับเบสแต่ละคู่ที่ได้กล่าวมาแล้ว ถ้าพิจารณาตามความแรงของกรดและเบสที่เข้าทำปฏิกิริยากัน แบ่งได้เป็น 4 ประภท และต้องเลือกใช้อินดิเคเตอร์ให้เหมาะสมสำหรับกรดกับเบสคู่นั้นๆดังนี้
การไทเทรตกรดกับเบสแต่ละคู่ที่ได้กล่าวมาแล้ว ถ้าพิจารณาตามความแรงของกรดและเบสที่เข้าทำปฏิกิริยากัน แบ่งได้เป็น 4 ประภท และต้องเลือกใช้อินดิเคเตอร์ให้เหมาะสมสำหรับกรดกับเบสคู่นั้นๆดังนี้1. การไทเทรตระหว่างกรดแก่และเบสแก่ ให้เลือกใช้อินดิเคเตอร์ที่แสดงจุดยุติที่pH ประมาณ 7
2. การไทเทรตระหว่างกรดแก่และเบสอ่อน ให้เลือกใช้อินดิเคเตอร์ที่แสดงจุดยุติที่ pH ต่ำกว่า 7
3. การไทเทรตระหว่างกรดอ่อนและเบสแก่ ให้เลือกใช้อินดิเคเตอร์ที่แสดงจุดยุติที่pH สูงกว่า 7
4. การไทเทตรระหว่างกรดอ่อนกับเบสอ่อน ให้เลือกใช้อินดิเคเตอร์ที่แสดงจุกยุติที่pH ประมาณ 7
ในกรณีที่ 4 จะมีการเปล่ยนแปลงค่า pH น้อยมาก เนื่องจากความอ่อนของทั้งกรดและเบส ทำให้ปฏิกิริยาเกิดขึ้นน้อย ดังนั้นการใช้อินดิเคเตอร์ที่มีการเปล่ยนแปลงสีที่จุดยุติ อาจทำให้สังเกตจุดยุติคลาดเคลื่อนได้ หรือบางกรณีไม่สามารถสังเกตจุดยุติได้ จึงต้องใช้ความระมัดระวังเป็นพิเศษในการไทเทรต

น.ส. ปัทมา ก๋งเม่ง รหัส 52050884
คณะวิทยาศาสตร์ สาขา เคมีทรัพยากรสิ่งแวดล้อม


ชอบอ่ามีรูปเยอะ555
ตอบลบงง
ตอบลบ